2.1 Sustancias simples e iones simples
Las sustancias simples son las que están formadas por un único tipo de átomo. Dentro de este tipo de sustancias podemos encontrar los metales (Fe, Cu, Pt), los gases monoatómicos (He, Ne) o las moléculas homonucleares (O2, Cl2, S6, P4, O3) sustancias formadas por un solo elemento, aunque puedan tener más de un átomo.
Los metales o los gases monoatómicos se nombran del mismo modo que el elemento que los compone. Diremos por tanto hierro (Fe), cobre (Cu), platino (Pt), helio (He) o neón (Ne). Las moléculas homonucleares se nombrarán usando el prefijo numeral que corresponda: dicloro (Cl2), hexaazufre (S6), tetrafósforo (P4). Excepciones a esta regla serán el oxígeno (O2) o el ozono (O3) que la IUPAC acepta como nombres correctos dado que su extensión en otras ramas del saber es muy amplia.
Ante la duda recomendamos que se use siempre el prefijo numeral, de ese modo se obtiene un nombre sistemático que es aceptado por la IUPAC: dioxígeno o trioxígeno son correctos.
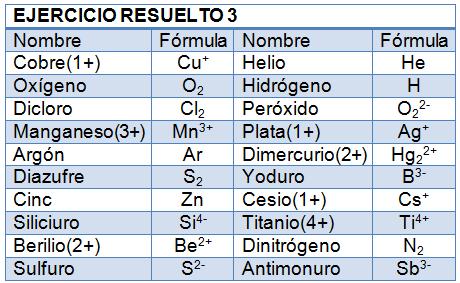
Nombrando sustancias simples
Completa la tabla:
| H | Octaazufre | ||
| Dinitrógeno | H2 | ||
| Diyodo | Oxígeno |
||
| Mg |
P4 |
||
| Diflúor | N |
Un ión (o ion) es una partícula que posee carga eléctrica. En nuestro caso puede ser un átomo o grupo de átomos. Si la carga es negativa decimos que se trata de un anión, mientras que si la carga es positiva hablamos de catión.
Los aniones monoatómicos se nombran empleando el sufijo -uro al final del nombre del átomo al que se le eliminan las últimas vocales. Es una excepción el oxígeno, que se nombra como óxido. La carga del anión se indica con el número de carga pero se puede omitir si el anión presenta una única carga. En la siguiente tabla se relacionan los nombres de los aniones monoatómicos:
| Fórmula | Nombre |
Fórmula |
Nombre |
| H- | Hidruro(1-) o hidruro |
Te2- | Telururo(3-) o telururo |
| F- | Fluoruro(1-) o fluoruro | N3- | Nitruro(3-) o nitruro |
| Cl- | Cloruro(1-) o cloruro |
P3- | Fosfuro(3-) o fosfuro |
| Br- | Bromuro(1-) o bromuro |
As3- | Arsenuro(3-) o arsenuro |
| I- | Yoduro(1-) o yoduro |
Sb3- | Antimonuro(3-) o antimonuro |
| O2- | Óxido(2-) u óxido |
C4- | Carburo(4-) o carburo |
| S2- | Sulfuro(2-) o sulfuro |
Si4- | Siliciuro(4-) o siliciuro |
| Se2- | Selenuro(2-) o selenuro |
B3- | Boruro(3-) o boruro |
En el caso de aniones homonucleares se usarán prefijos numerales que hagan referencia al número de átomos que componen el anión. Hay algunos nombres comunes para estos aniones que son aceptados por la IUPAC y que debemos conocer:
| Fórmula | Nombre sistemático |
Nombre aceptado |
| O2- | Dióxido(1-) | Superóxido |
| O22- | Dióxido(2-) | Peróxido |
| I3- | Triyoduro(1-) | |
| C22- | Dicarburo(2-) | Acetiluro |
| S22- | Disulfuro(2-) | |
Los cationes monoatómicos se nombran usando el nombre del elemento y el número de carga. Para los cationes no se debe omitir el número de carga aunque sea único: Na+ [sodio(1+)] ; Ni2+ [níquel(2+)] ; Ni3+ [níquel(3+)] ; Ca2+ [calcio(2+)].
Cuando se trata de cationes homonucleares habrá que usar el prefijo numeral que indique el número de átomos que constituye el catión y el número de carga. El catión más común de este tipo es el Hg22+ [dimercurio(2+)].
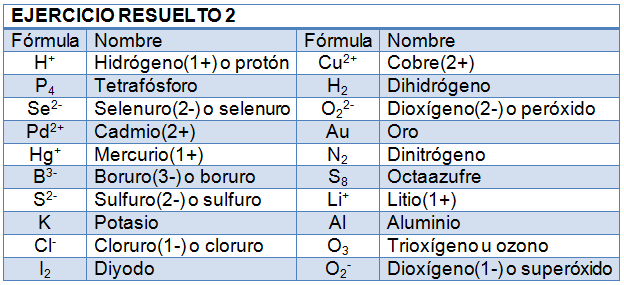
Nombrando iones
Copia la tabla en tu libreta y complétala:
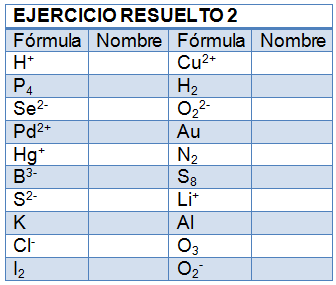
¡Practica la formulación!
Completa la tabla siguiente: