-
Variación de los puntos de fusión y ebullición del agua cuando se mezcla con glicerina (5167)
Una solución acuosa tiene una densidad de 1.05 g/mL y contiene 0.200 kg de glicerina (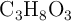 ) disueltos en 800 g de agua, a 1 atm de presión. ¿Cuál es el intervalo de temperatura en el que la solución se mantiene líquida?
) disueltos en 800 g de agua, a 1 atm de presión. ¿Cuál es el intervalo de temperatura en el que la solución se mantiene líquida?
Datos: 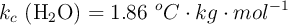 ;
; 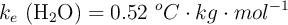
-
Temperatura de fusión de una disolución de ácido cítrico (5146)
Calcula el punto de congelación de una solución que contiene 17.25 g de ácido cítrico (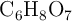 ) disueltos en 250 g de agua. La constante crioscópica del agua es
) disueltos en 250 g de agua. La constante crioscópica del agua es 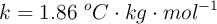 .
.
-
Descenso de la presión de vapor del disolvente al añadir un soluto (5119)
A temperatura muy próxima a 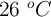 , la presión de vapor del agua resulta ser de 25.21 mm Hg. Calcula la presión de vapor a la misma temperatura de una solución de 2.32 molal de un compuesto no electrólitico y no volátil, suponiendo comportamiento ideal.
, la presión de vapor del agua resulta ser de 25.21 mm Hg. Calcula la presión de vapor a la misma temperatura de una solución de 2.32 molal de un compuesto no electrólitico y no volátil, suponiendo comportamiento ideal.
-
Descenso de la presión de vapor en una disolución
¿Cuál será la presión de vapor de una solución a 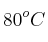 , si se preparó con 32 gramos cloruro de calcio (
, si se preparó con 32 gramos cloruro de calcio (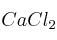 ) en 800 g de agua. La presión de vapor del agua a esa temperatura es de 355,1 mmHg.
) en 800 g de agua. La presión de vapor del agua a esa temperatura es de 355,1 mmHg.
Masas atómicas: Ca = 40 ; Cl = 35,5 ; H = 1 ; O = 16.
-
Presión osmótica de una disolución diluida (4935)
Calcula la presión osmótica de una disolución de concentración 0.10 M, cuando la temperatura de la misma es de 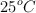 .
.
 Propiedades coligativas
Propiedades coligativas