-
Volumen ocupado por gases en condiciones normales (2399)
Calcula el volumen de:
a) 30 g de 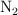 en condiciones normales de P y T.
en condiciones normales de P y T.
b) 1.01 moles de 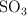 en condiciones normales de P y T.
en condiciones normales de P y T.
c) 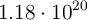 moléculas de
moléculas de 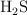 en condiciones normales de P y T.
en condiciones normales de P y T.
-
Ley de Boyle-Mariotte (2374)
Cierta cantidad de gas ocupa un volumen de 34 mL a la presión de 200 mm de Hg. ¿Qué volumen ocupará a la presión de 840 mm de Hg?
-
Presión de un gas que aumenta su temperatura a volumen constante (2373)
Una muestra de gas ocupa un volumen de 44.8 litros en condiciones estándar, es decir, a 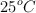 de temperatura y una presión de una atmósfera. ¿Cuál será su presión a una temperatura de
de temperatura y una presión de una atmósfera. ¿Cuál será su presión a una temperatura de 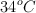 , manteniendo el volumen constante?
, manteniendo el volumen constante?
-
Temperatura que alcanza un gas que duplica su volumen a presión constante (2364)
Isobáricamente, el volumen de un gas se duplica. Si la temperatura inicial es 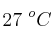 , calcula la temperatura final.
, calcula la temperatura final.
-
Ley de Gay-Lussac: temperatura inicial de un gas que se calienta y aumenta su presión (2363)
Se coloca un gas ideal en un recipiente cerrado. Cuando la temperatura aumenta en diez grados, la presión aumenta un 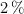 . Indica la temperatura inicial expresada en escala Celsius.
. Indica la temperatura inicial expresada en escala Celsius.
 Leyes de los gases
Leyes de los gases