-
Reacción entre el SO2 y el O2 para dar SO3 (6975)
Durante la fabricación del ácido sulfúrico, el dióxido de azufre (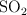 ) se hace reaccionar con oxígeno (
) se hace reaccionar con oxígeno (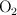 ) para obtener trióxido de azufre (
) para obtener trióxido de azufre (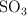 ), también gas.
), también gas.
a) Escribe y ajusta la reacción que tiene lugar.
b) ¿Cuántos gramos de oxígeno hacen falta para reaccionar con 16 g de 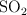 ?
?
c) ¿Cuántos gramos de 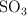 se obtendrán en ese caso?
se obtendrán en ese caso?
-
Reactivo limitante y productos obtenidos en la tostación de la pirita (6886)
La pirita es un mineral compuesto de hierro y azufre, cuya fórmula es 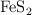 y que se hace reaccionar con gas oxígeno, para dar lugar a óxido de hierro(III) y óxido de azufre(IV). Sabiendo que tenemos 500 g de pirita, que tiene una riqueza del
y que se hace reaccionar con gas oxígeno, para dar lugar a óxido de hierro(III) y óxido de azufre(IV). Sabiendo que tenemos 500 g de pirita, que tiene una riqueza del 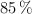 en
en 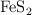 , y que reacciona con 300 L de aire (con un
, y que reacciona con 300 L de aire (con un 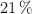 en volumen de oxígeno).
en volumen de oxígeno).
a) Identifica el reactivo limitante.
b) Calcula los gramos de óxido de hierro(III) que aparecen al producirse la reacción.
c) Calcula los litros de óxido de azufre(IV) que se producen.
Datos: 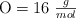 ;
; 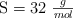 ;
; 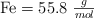 ;
; 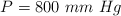 ;
; 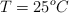 ;
; 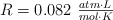
-
Porcentaje de alcohol en sangre para saber si se incumple la ley (6739)
El alcohol contenido en una muestra de 10.0 g de sangre de un conductor necesitó 4.23 mL de 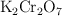 0.07654 M para su valoración. ¿Podría la policía procesar al individuo por conducir ebrio, sabiendo que el límite está en un
0.07654 M para su valoración. ¿Podría la policía procesar al individuo por conducir ebrio, sabiendo que el límite está en un 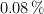 ?
?
-
Masa de NaOH necesaria y masa de NaNO3 formada en la neutralización del HNO3 (6690)
¿Qué masa de 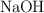 reaccionará con 20 g de
reaccionará con 20 g de 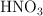 (ácido nítrico) y cuántos gramos y moles de
(ácido nítrico) y cuántos gramos y moles de 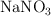 se formarán en la reacción de neutralización?
se formarán en la reacción de neutralización?
-
Reacción entre hierro y vapor de agua para dar Fe3O4 e hidrógeno (6626)
En la reacción de hierro metálico con vapor de agua se produce óxido ferroso- férrico (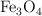 ) e hidrógeno molecular.
) e hidrógeno molecular.
a) Formula y ajusta la reacción química que tiene lugar.
b) Calcula el volumen de hidrógeno gaseoso medido a 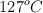 y 5 atm que se obtiene por reacción de 558 g de hierro metálico.
y 5 atm que se obtiene por reacción de 558 g de hierro metálico.
c) ¿Cuántos gramos de óxido ferroso-férrico se obtendrán a partir de 3 moles de hierro?
d) ¿Cuántos litros de vapor de agua a 10 atm y 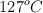 se precisan para reaccionar con los 3 moles de hierro?
se precisan para reaccionar con los 3 moles de hierro?
Datos: Fe = 55.8 ; O = 16 ; 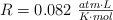
 Reacciones químicas
Reacciones químicas