Calcula la longitud de onda asociada a una partícula alfa, (su masa es 4 u), que posee una energía de ![]()
Datos: ![]() ;
; ![]()
Problemas, ejercicios y cuestiones sobre modelos atómicos, configuraciones electrónicas, propiedades periódicas y otros temas relacionados con la materia y su estructura.
Calcula la longitud de onda asociada a una partícula alfa, (su masa es 4 u), que posee una energía de ![]()
Datos: ![]() ;
; ![]()
¿Cuál será la energía de ionización del átomo de hidrógeno?
Datos: 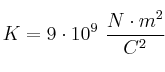 ;
; ![]() ;
; ![]() ;
; ![]() ;
; ![]()
¿Qué línea de la serie de Lyman aparece a una longitud de onda de 97 nm?
La energía umbral de cierto metal es $$$ 8.2\cdot 10^{-19}\ \text{J}$$$. Si la longitud de onda de una radiación incidente es de $$$ 2\ 000\ \mathring{A}$$$, ¿se producirá efecto fotoeléctrico? ¿Cuál sería la energía cinética asociada a los electrones?
El ![]() del nitrógeno es
del nitrógeno es ![]() (masa isotópica 14.0031 u) y el resto es
(masa isotópica 14.0031 u) y el resto es ![]() (masa isotópica 15.0010 u). Determina el peso atómico del nitrógeno.
(masa isotópica 15.0010 u). Determina el peso atómico del nitrógeno.