¿Qué masa de ![]() se forma en la reacción de 125 g de
se forma en la reacción de 125 g de ![]() con 323 g de
con 323 g de ![]() ?
?
La reacción que tiene lugar es:
![]()
El aluminio y el bromo reaccionan según la reacción:
![]()
Se usan en la reacción 16 g de aluminio y 100 g de bromo, ¿cuál es la masa de reactivo sobrante?
Masas atómicas: Al = 27 y Br = 80.
¿Cuántos gramos de cloruro de sodio se obtienen a partir de la reacción de 15 g de hidróxido de sodio, cuando reaccionan con exceso de HCl?
¿Cuántos gramos de dióxido de carbono se obtienen a partir de la reacción de 10 g de carbono cuando reaccionan con exceso de oxígeno? La reacción que tiene lugar es: ![]()
En la reacción de formación de amoniaco (![]() ), tenemos 50 litros de nitrógeno y 100 litros de hidrógeno,con P = 1 atm y T = 283 K. ¿Cuántos litros de amoniaco se obtienen?
), tenemos 50 litros de nitrógeno y 100 litros de hidrógeno,con P = 1 atm y T = 283 K. ¿Cuántos litros de amoniaco se obtienen?
Dadas las siguientes ecuaciones químicas no balanceadas:
a) ![]()
b) ![]()
c) ![]()
¿Cuál de las reacciones conviene utilizar para, partiendo de iguales masas de reactivos, obtener la máxima cantidad posible de dióxido de carbono?
Teniendo la siguiente reacción de combustión del monóxido de carbono:
![]()
si se hacen reaccionar 150 L de ![]() y se obtienen 255 L de
y se obtienen 255 L de ![]() , ¿cuál es el rendimiento de la reacción?
, ¿cuál es el rendimiento de la reacción?
Analiza los siguientes datos sobre la descomposición del peróxido de hidrógeno y responde a las preguntas:
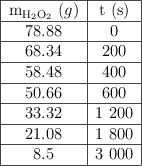
a) Calcula la rapidez de la reacción para cada uno de los tiempos de la tabla.
b) Calcula la rapidez promedio de la reacción.
c) Determina la rapidez instantánea de la reacción para el tiempo 1 000 s.
¿Qué volumen, en condiciones normales, de gas acetileno (![]() ) se puede obtener haciendo reaccionar 640 g de carburo de calcio (
) se puede obtener haciendo reaccionar 640 g de carburo de calcio (![]() ) con agua.
) con agua.
Datos: Ca = 40 ; O = 16 ; H = 1 ; C = 12
Si se hicieran reaccionar 4.50 L de ![]() con 4.50 L de
con 4.50 L de ![]() , ambos a
, ambos a ![]() y 720 torr. ¿Qué volumen de amoniaco gaseoso,
y 720 torr. ¿Qué volumen de amoniaco gaseoso, ![]() , se produciría a
, se produciría a ![]() y 720 torr?
y 720 torr?
 Ejercicios FyQ
Ejercicios FyQ