Un disco de aluminio de 123 g a ![]() absorbe 456 calorías. ¿Cuál será la temperatura final que alcance? Considera que el calor específico del aluminio es
absorbe 456 calorías. ¿Cuál será la temperatura final que alcance? Considera que el calor específico del aluminio es ![]() .
.
Un alambre de cobre mide 10 cm y al calentarlo se dilata, llegando a medir 10.2 cm. ¿Cuál habrá sido el aumento de temperatura que ha sufrido?
Dato: ![]()
Considera una masa de 200 kg de agua que cae de lo alto de una catarata cuya altura es de 210 m.
Cuando el agua choca con el suelo su energía cinética se transforma casi totalmente en energía interna, produciendo un aumento de temperatura. Suponiendo que toda energía cinética haya sido empleada para calentar agua, ¿cuanto se elevaría su temperatura?
Dato: ![]()
Cierta cantidad de agua se calentó desde ![]() hasta
hasta ![]() . Si el calor necesario para calentar el agua fue 15 400 cal. ¿Cuántos kilogramos de agua había en la vasija?
. Si el calor necesario para calentar el agua fue 15 400 cal. ¿Cuántos kilogramos de agua había en la vasija?
Se tienen 20 g de vapor de agua a ![]() . Determina el calor que hay que extraer para condensarlos completamente.
. Determina el calor que hay que extraer para condensarlos completamente.
Datos: ![]() ;
; ![]()
250 g de una sustancia A se encuentran en estado líquido a ![]() . ¿Qué cantidad de calor hemos de transferir para enfriar la sustancia A a
. ¿Qué cantidad de calor hemos de transferir para enfriar la sustancia A a ![]() ?
?
Datos: ![]() ;
; ![]() ;
; ![]() ;
; ![]()
Una masa de 250 g de una sustancia eleva su temperatura de ![]() a
a ![]() . Si su calor específico es
. Si su calor específico es ![]() . ¿Qué cantidad de calor absorbió?
. ¿Qué cantidad de calor absorbió?
Determina la cantidad de calor que cedieron 20 kg de agua para enfriarse desde los ![]() hasta los
hasta los ![]() .
.
Datos: ![]() ;
; 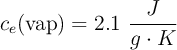 ;
; 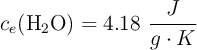 ;
; 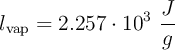
La evaporación del agua en la piel es un mecanismo importante para controlar la temperatura del cuerpo debido al valor tan elevado del calor latente de vaporización del agua (![]() ). Calcula la rapidez con que pierde calor una persona que suda 2.2 kg de agua haciendo ejercicio físico durante una hora.
). Calcula la rapidez con que pierde calor una persona que suda 2.2 kg de agua haciendo ejercicio físico durante una hora.
Un trozo de material «X», que tiene una masa igual a 27.305 g, se calienta hasta ![]() y se sumerge luego en
y se sumerge luego en ![]() de agua a
de agua a ![]() . Si la temperatura final del sistema es
. Si la temperatura final del sistema es ![]() , determina el calor específico del material «X».
, determina el calor específico del material «X».
![]() ;
; ![]()
 Ejercicios FyQ
Ejercicios FyQ