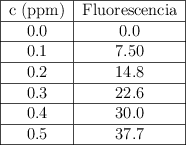
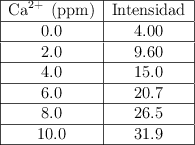
Se desea determinar la concentración de una solución acuosa de iones permanganato (![]() ) mediante espectrofotometría UV-Vis. Para ello, se prepara una curva de calibración midiendo la absorbancia de cinco disoluciones estándar de
) mediante espectrofotometría UV-Vis. Para ello, se prepara una curva de calibración midiendo la absorbancia de cinco disoluciones estándar de ![]() en una cubeta de 1.00 cm de camino óptico. Los datos obtenidos son los siguientes:
en una cubeta de 1.00 cm de camino óptico. Los datos obtenidos son los siguientes:
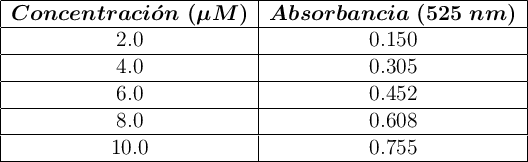
Posteriormente, se mide la absorbancia de una muestra problema diluida 1:5, obteniéndose un valor de 0.523.
a) Determina la ecuación de la curva de calibración y calcula la absortividad molar (![]() ) del
) del ![]() a 525 nm.
a 525 nm.
b) Calcula la concentración de ![]() en la muestra original (antes de la dilución).
en la muestra original (antes de la dilución).
 EjerciciosFyQ
EjerciciosFyQ