Calcula la molalidad de una disolución formada por 54 g de glucosa (![]() ) en 600 mL de agua.
) en 600 mL de agua.
Masas atómicas: C = 12 ; O = 16 y H = 1.
Al mezclar 30 g de glucosa (![]() ) con 150 g de agua se obtienen 178 mL de disolución. Calcula la molalidad de la disolución.
) con 150 g de agua se obtienen 178 mL de disolución. Calcula la molalidad de la disolución.
Masas atómicas: C = 12 ; H = 1 ; O = 16.
¿Cuál es la molalidad de una solución con 400 g de glucosa (![]() ) en 1 litro de agua?
) en 1 litro de agua?
Calcula la molalidad de una disolución acuosa de ![]() 0.15 M cuya densidad es
0.15 M cuya densidad es ![]() .
.
Se quieren disolver 720 mg de yodo (![]() ) en 850 mL de tetracloruro de carbono cuya densidad es de
) en 850 mL de tetracloruro de carbono cuya densidad es de ![]() . ¿Cuál es la concentración molal de la disolución?
. ¿Cuál es la concentración molal de la disolución?
Determina la concentracion molal de una solución de ![]() sabiendo que la masa de soluto es 180 g y se diluye en 3 kg de solución.
sabiendo que la masa de soluto es 180 g y se diluye en 3 kg de solución.
Masas atómicas: Ba = 137 ; O = 16 ; H = 1.
Se disuelven 3,5 g de ácido sulfúrico en 500 g de agua. Si la densidad de la disolución resultante es 1,5 g/mL, expresa la concentración de la solución en:
a) molalidad
b) molaridad
Si el punto de ebullición de una disolución de sacarosa (![]() ) es
) es ![]() , ¿cuáles serán su molalidad y su porcentaje en masa?
, ¿cuáles serán su molalidad y su porcentaje en masa?
Datos: ![]() ; C = 12 ; H = 1 ; O =16.
; C = 12 ; H = 1 ; O =16.
A ![]() la solubilidad de la urea
la solubilidad de la urea ![]() es de
es de ![]() . Averigua:
. Averigua:
a) La molalidad de la solución saturada, sabiendo que la densidad del etanol a ![]() es
es ![]() .
.
b) El porcentaje en peso 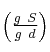 y el porcentaje en peso
y el porcentaje en peso ![]() .
.
Masas atómicas: H = 1 ; C = 12 ; N = 14 ; O = 16.
(Recuerda que S es soluto, d es disolvente y D es disolución).
Calcula la molaridad de una disolución de ácido sulfuroso cuya concentración es ![]() (m/V).
(m/V).
 Ejercicios FyQ
Ejercicios FyQ