Escribe las reacciones de disociación de los siguientes compuestos: a) ácido nítrico; b) hidróxido de cinc; c) ácido perbrómico; d) hidróxido de cobre(II); e) ácido antimonioso.
Ejercicios y problemas sobre reacciones químicas: estequiometría, ajuste de reacciones químicas y cálculos estequiométricos.
Escribe las reacciones de disociación de los siguientes compuestos: a) ácido nítrico; b) hidróxido de cinc; c) ácido perbrómico; d) hidróxido de cobre(II); e) ácido antimonioso.
El hidrógeno y el oxígeno gaseosos reaccionan, en condiciones adecuadas, dando agua líquida. Si se hacen reaccionar 10 L de ![]() con 3.5 L de
con 3.5 L de ![]() medidos en condiciones normales, ¿qué masa de agua se obtendrá?
medidos en condiciones normales, ¿qué masa de agua se obtendrá?
Masas atómicas: H = 1 ; O = 16.
Si se hicieran reaccionar 4.50 L de ![]() con 4.50 L de
con 4.50 L de ![]() , ambos a
, ambos a ![]() y 720 torr. ¿Qué volumen de amoniaco gaseoso,
y 720 torr. ¿Qué volumen de amoniaco gaseoso, ![]() , se produciría a
, se produciría a ![]() y 720 torr?
y 720 torr?
Analiza los siguientes datos sobre la descomposición del peróxido de hidrógeno y responde a las preguntas:
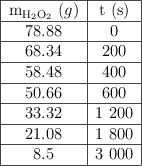
a) Calcula la rapidez de la reacción para cada uno de los tiempos de la tabla.
b) Calcula la rapidez promedio de la reacción.
c) Determina la rapidez instantánea de la reacción para el tiempo 1 000 s.
La razón entre las masas de A y B es 0.125. ¿Qué masa de compuesto C se formará al poner en contacto 25.0 g de A con 75.0 g de B?